酸、堿���、鹽知識(shí)點(diǎn)匯總及解析
作者: 日期:2024-05-27 來源: 關(guān)注:33
酸�、堿、鹽的知識(shí)點(diǎn)是初中化學(xué)最難的一部分了����,今天小編把初中化學(xué)的酸、堿�����、鹽知識(shí)點(diǎn)做了一個(gè)匯總��,快轉(zhuǎn)給孩子吧����!
一、酸��、堿、鹽的組成
酸是由氫元素和酸根組成的化合物 如:佛山工業(yè)硫酸(H2SO4)���、佛山工業(yè)鹽酸(HCl)�、硝酸(HNO3)
堿是由金屬元素和氫氧根組成的化合物 如:氫氧化鈉�����、氫氧化鈣��、氨水(NH3·H2O)
鹽是由金屬元素元素(或銨根)和酸根組成的化合物 如:氯化鈉�����、碳酸鈉
酸����、堿����、鹽的水溶液可以導(dǎo)電(原因:溶于水時(shí)離解形成自由移動(dòng)的陰、陽離子)
二�����、酸
1、濃鹽酸�、濃硫酸的物理性質(zhì)、特性�、用途
| 濃鹽酸 | 濃硫酸 |
顏色、狀態(tài) | “純凈”:無色液體工業(yè)用鹽酸:黃色(含F(xiàn)e3+) | 無色粘稠���、油狀液體 |
氣味 | 有刺激性氣味 | 無 |
特性 | 揮發(fā)性(敞口置于空氣中����,瓶口有白霧) | 吸水性 脫水性強(qiáng)氧化性 腐蝕性 |
用途 | ①金屬除銹②制造藥物③人體中含有少量鹽酸��,助消化 | ①金屬除銹②濃硫酸作干燥劑③生產(chǎn)化肥��、精煉石油 |
2���、酸的通性(具有通性的原因:酸離解時(shí)所生成的陽離子全部是H+)
(1)與酸堿指示劑的反應(yīng):使紫色石蕊試液變紅色��,不能使無色酚酞試液變色
(2)金屬 + 酸 → 鹽 + 氫氣
(3)堿性氧化物 + 酸 → 鹽 + 水
(4)堿 + 酸 → 鹽 + 水
(5)鹽 + 酸 → 另一種鹽 + 另一種酸(產(chǎn)物符合復(fù)分解條件)
3�、三種離子的檢驗(yàn)
| 試劑 |
Cl- | AgNO3 及HNO3 |
SO42- | ①Ba(NO3)2及HNO3②HCl 及BaCl2 |
CO32- | HCl 及石灰水 |
三�����、堿
1��、氫氧化鈉、氫氧化鈣的物理性質(zhì)���、用途
| 氫氧化鈉 | 氫氧化鈣 |
顏色�、狀態(tài) | 白色固體��,極易溶于水(溶解放熱) | 白色粉末����,微溶于水 |
俗名 | 燒堿、火堿���、苛性鈉(具有強(qiáng)腐蝕性) | 熟石灰、消石灰 |
制法 | Ca(OH)2+Na2CO3== CaCO3↓+2NaOH | CaO +H2O== Ca(OH)2 |
用途 | ①氫氧化鈉固體作干燥劑②化工原料:制肥皂����、造紙③去除油污:爐具清潔劑中含氫氧化鈉 | ①工業(yè):制漂白粉②農(nóng)業(yè):改良酸性土壤、配波爾多液③建筑: |
2����、堿的通性(具有通性的原因:離解時(shí)所生成的陰離子全部是OH-)
(1)堿溶液與酸堿指示劑的反應(yīng):使紫色石蕊試液變藍(lán)色,使無色酚酞試液變紅色
(2)酸性氧化物+堿 → 鹽+水
(3)酸+堿 → 鹽+水
(4)鹽+堿 → 另一種鹽+另一種堿(反應(yīng)物均可溶�����,產(chǎn)物符合復(fù)分解條件)
注:①難溶性堿受熱易分解(不屬于堿的通性)
如Cu(OH)2 ΔCuO +H2O
2Fe(OH)3 ΔFe2O3+3H2O
②常見沉淀:AgCl↓ BaSO4↓ Cu(OH)2↓ F e(OH)3↓ Mg(OH)2↓ BaCO3↓ CaCO3↓
③復(fù)分解反應(yīng)的條件:當(dāng)兩種化合物互相交換成分,生成物中有沉淀或有氣體或有水生成時(shí)��,復(fù)分解反應(yīng)才可以發(fā)生�����。
四�����、酸性氧化物與堿性氧化物
| 酸性氧化物 | 堿性氧化物 |
定義 | 凡能與堿反應(yīng)生成鹽和水的氧化物大多數(shù)非金屬氧化物是酸性氧化物大多數(shù)酸性氧化物是非金屬氧化物 | 凡能與酸反應(yīng)生成鹽和水的氧化物大多數(shù)金屬氧化物是堿性氧化物所有堿性氧化物是金屬氧化物 |
化學(xué)性質(zhì) | (1)大多數(shù)可與水反應(yīng)生成酸CO2+H2O== H2CO3SO2+H2O== H2SO3SO3+H2O== H2SO4 | (1)少數(shù)可與水反應(yīng)生成堿Na2O +H2O== 2NaOHK2O +H2O== 2KOHBaO +H2O== Ba(OH)2CaO +H2O== Ca(OH)2 |
(2) 酸性氧化物+堿 → 鹽+水CO2 +Ca(OH)2== CaCO3↓+H2O(不是復(fù)分解反應(yīng)) | (2) 堿性氧化物+酸 → 鹽+水Fe2O3+6HCl== 2FeCl3+3H2O |
|
五�����、中和反應(yīng) 溶液酸堿度的表示法--pH
1�、定義:酸與堿作用生成鹽和水的反應(yīng)
2、應(yīng)用:
(1)改變土壤的酸堿性
(2)處理工廠的廢水
(3)用于醫(yī)藥
3�、溶液酸堿度的表示法--pH
(1)
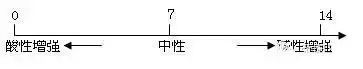
(2)pH的測(cè)定:最簡(jiǎn)單的方法是使用pH試紙
用玻璃棒(或滴管)蘸取待測(cè)試液少許,滴在pH試紙上�����,顯色后與標(biāo)準(zhǔn)比色卡對(duì)照�����,讀出溶液的pH(讀數(shù)為整數(shù))
(3)酸雨:正常雨水的pH約為5.6(因?yàn)槿苡蠧O2)
pH<5.6的雨水為酸雨
酸的組成——?dú)潆x子+酸根離子
(1)跟指示劑反應(yīng)
紫色石蕊試液遇酸變紅色
無色酚酞試液遇酸不變色
(2)酸的PH<7
(3)跟(H)前的活潑金屬起置換反應(yīng)
酸 + 金屬==鹽 + 氫氣
例:2HCl+Fe=FeCl2+H2↑
(4) 跟堿性氧化物和某些金屬氧化物反應(yīng)
酸 + 堿性(金屬)氧化物—→鹽+水
例:3H2SO4+Fe2O3=Fe2(SO4)3+3H2O
(5)跟某些鹽反應(yīng)
酸+碳酸鹽==鹽+水
酸+鹽—→新酸+新鹽
例:H2SO4+BaCl2=2HCl+BaSO4↓
(6)跟堿起中和反應(yīng)
酸+堿—→鹽+水
例:2HCl+Cu(OH)2=CuCl2+2H2O
在各省市中考試卷的命題中,無不將酸堿鹽的化學(xué)性質(zhì)的考察作為重中之重�����。其題型之多變化之大�����,對(duì)于同學(xué)們來講確有千頭萬緒��、力不從心之感���?���;诖?���,筆者結(jié)合教學(xué)實(shí)踐淺談一下有關(guān)酸堿鹽的復(fù)習(xí)�,以期對(duì)同學(xué)們的復(fù)習(xí)有所助益。
一���、熟練記憶規(guī)律是應(yīng)用的前提
酸堿鹽部分雖然題型眾多��,如:鑒別���、推斷�、除雜……�,但是這些應(yīng)用離不開最基礎(chǔ)的知識(shí)點(diǎn):即:對(duì)酸堿鹽化學(xué)性質(zhì)的熟練記憶。
通過學(xué)習(xí)可知:酸的通性有五點(diǎn)�����、堿和鹽的通性各有四點(diǎn)��。對(duì)于這些化學(xué)性質(zhì)必須加以強(qiáng)化記憶和靈活記憶�����?����?刹捎脠D表記憶法以及變式記憶法等���。
如:將酸堿鹽的化學(xué)性質(zhì)濃縮為下圖記憶較好(圖表記憶法)
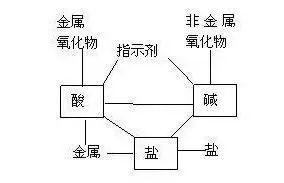
在此基礎(chǔ)上�����,再做變式練習(xí)���,增加對(duì)化學(xué)性質(zhì)的多角度記憶(變式記憶法)����。如:
(1)生成鹽和水的規(guī)律��,一定是中和反應(yīng)嗎���?
(2)在酸堿鹽的化學(xué)性質(zhì)中��,生成鹽的規(guī)律有幾條等�。
通過如上練習(xí)�����,即可起到加強(qiáng)知識(shí)的同化和異化的作用���。
二、掌握“規(guī)矩”�����,可成“方圓”
記憶住以上規(guī)律就可以熟練應(yīng)用了嗎?當(dāng)然不能��。在大量練習(xí)中同學(xué)們發(fā)現(xiàn)以上規(guī)律中有很多是有 “規(guī)矩” 有條件的�。因此在記住規(guī)律的前提下,還要記住規(guī)律應(yīng)用的條件�,這樣才能做到有的放矢的應(yīng)用。比如:可根據(jù)不同反應(yīng)類型來靈活記憶有關(guān)反應(yīng)的條件����。歸納如下:
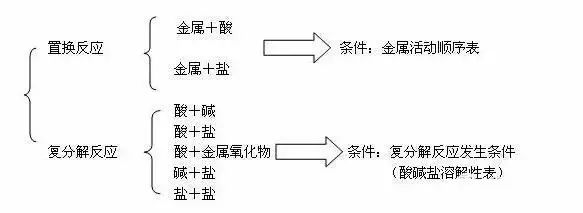
三、抓重點(diǎn)題型����,學(xué)會(huì)以點(diǎn)帶面
在復(fù)習(xí)中經(jīng)常見到不少同學(xué)埋頭于題海之中,耗時(shí)長(zhǎng)收效甚微���。酸堿鹽部分的題型雖形式多樣��,但萬變不離其宗���。綜合之下,可以說鑒別���、除雜��、推斷這三類題型是很具代表性的����,它們的正確理解和掌握,對(duì)于提高其他相關(guān)題型的應(yīng)變能力��,必將起到很好的輻射作用�。
初三化學(xué):
有關(guān)酸堿鹽的化學(xué)方程式
單質(zhì)、氧化物����、酸、堿����、鹽的相互關(guān)系
(1)金屬單質(zhì) + 酸 --- 鹽 + 氫氣 (置換反應(yīng))
1. 鋅和稀硫酸Zn + H2SO4 = ZnSO4 + H2↑ (最常用)
(實(shí)驗(yàn)室制H2用的金屬有Zn,Fe,Mg,Al,酸有稀H2SO4和稀HCl )
(2)金屬單質(zhì) + 鹽(溶液) --- 另一種金屬 + 另一種鹽
2. 鐵和硫酸銅溶液反應(yīng):Fe + CuSO4 = FeSO4 + Cu
3. 鋁和硝酸銀溶液反應(yīng):Al+ 3AgNO3 = Al(NO3)3 + 3Ag
(3)堿性氧化物(金屬氧化物) +酸 --- 鹽 + 水
4. 氧化鐵和稀硫酸反應(yīng):Fe2O3 + 3H2SO4 = Fe2(SO4)3 + 3H2O
5. 氧化鈣和稀鹽酸反應(yīng):CaO + 2HCl = CaCl2 + H2O
(4)酸性氧化物(非金屬氧化物) +堿 -------- 鹽 + 水
6.苛性鈉暴露在空氣中變質(zhì):2NaOH + CO2 = Na2CO3 + H2O
7.消石灰放在空氣中變質(zhì):Ca(OH)2 + CO2 = CaCO3 ↓+ H2O
(5)酸 + 堿 -------- 鹽 + 水 (中和反應(yīng))
8.鹽酸和燒堿反應(yīng):HCl + NaOH = NaCl +H2O
9. 鹽酸和氫氧化鈣反應(yīng):2HCl + Ca(OH)2 = CaCl2 + 2H2O
10.氫氧
(6)酸 + 鹽 -------- 另一種酸 + 另一種鹽
11.大理石與稀鹽酸反應(yīng):CaCO3 + 2HCl = CaCl2 + H2O + CO2↑ (實(shí)驗(yàn)室制CO2)
12.碳酸鈉與稀鹽酸反應(yīng): Na2CO3 + 2HCl = 2NaCl + H2O + CO2↑
13.硫酸和氯化鋇溶液反應(yīng):H2SO4 + BaCl2 = BaSO4 ↓+ 2HCl
(7)堿 + 鹽 --- 另一種堿 + 另一種鹽
14. 氫氧化鈣與碳酸鈉:Ca(OH)2 + Na2CO3 = CaCO3↓+ 2NaOH
15.硫酸銅溶液與氫氧化鋇:CuSO4 + Ba(OH)2 = BaSO4↓+ Cu(OH)2↓
(8)鹽 + 鹽 --- 兩種新鹽
16.氯化鈉溶液和硝酸銀溶液:NaCl + AgNO3 = AgCl↓ + NaNO3
17.硫酸鈉和氯化鋇:Na2SO4 + BaCl2 = BaSO4↓ + 2NaCl
復(fù)分解反應(yīng)必須生成沉淀��,氣體或水生成才能發(fā)生�����,且生成物的元素化合價(jià)不變�。
+1價(jià):HClO ;NaClO��;Ca(ClO)2.
+5價(jià):HClO3 ���;KClO3.
+7價(jià):HClO4 ���;KClO4.
化學(xué)酸堿鹽輔導(dǎo):
果相同,因有異
初中化學(xué)第八章中��,存在著一些結(jié)果(結(jié)論)相同����、原因有異的問題,現(xiàn)圍繞酸���、堿的有關(guān)知識(shí)���,選取幾例加以分析。
1.酸����、堿溶液和金屬都能導(dǎo)電。
分析:酸����、堿溶液導(dǎo)電的原因是��,酸�、堿溶液中含有自由移動(dòng)的離子(其中酸溶液中含有自由移動(dòng)的氫離子和酸根離子����;堿溶液中含有自由移動(dòng)的金屬離子和氫氧根離子);金屬導(dǎo)電的原因是��,金屬中含有自由移動(dòng)的電子���。
2.濃硫酸����、濃鹽酸敞口置于空氣中����,溶液中溶質(zhì)質(zhì)量分?jǐn)?shù)都變小。
分析:濃硫酸中溶質(zhì)質(zhì)量分?jǐn)?shù)之所以變小�����,是因?yàn)闈饬蛩峋哂形?�,濃硫酸吸收空氣中的水分?dǎo)致了溶液中溶劑量的增加;濃鹽酸中溶質(zhì)質(zhì)量分?jǐn)?shù)之所以變小�,是因?yàn)闈恹}酸具有揮發(fā)性,氯化氫氣體的揮發(fā)導(dǎo)致了溶液中溶質(zhì)質(zhì)量的減少����。
3.濃硫酸��、氫氧化鈉溶于水����,生石灰放入水中,都能放出大量的熱�。
分析:濃硫酸、氫氧化鈉溶于水放熱�����,屬于溶解過程中的放熱現(xiàn)象�����;生石灰與水接觸放熱�����,屬于化學(xué)變化(生石灰與水發(fā)生化學(xué)反應(yīng),生成氫氧化鈣)中的放熱現(xiàn)象���。
4.金屬鈉和鎂放入稀鹽酸中�����,都有氫氣放出��。
分析:金屬鈉放入稀鹽酸中所放出的氫氣�����,主要是由鈉與水發(fā)生置換反應(yīng)產(chǎn)生的(在金屬活動(dòng)順序表中名列第三的金屬鈉��,其化學(xué)性質(zhì)非?;顫?�,能在常溫下與水發(fā)生劇烈反應(yīng):2Na+2H2O==2NaOH+H2↑)����;鎂放入稀鹽酸中所產(chǎn)生的氫氣,是鎂和稀鹽酸發(fā)生置換反應(yīng)產(chǎn)生的��。
5.氫氧化鈉溶液與硫酸銅溶液�����、稀鹽酸與碳酸鈉溶液發(fā)生反應(yīng)(假設(shè)兩個(gè)反應(yīng)都恰好完全發(fā)生)后,溶液的總質(zhì)量都減少��。
分析:根據(jù)上述變化的化學(xué)方程式以及質(zhì)量守恒定律可以得出����,前一個(gè)反應(yīng)后所得溶液的質(zhì)量==氫氧化鈉溶液的質(zhì)量+硫酸銅溶液的質(zhì)量-生成的氫氧化銅沉淀的質(zhì)量��;后一個(gè)反應(yīng)后所得溶液的質(zhì)量==稀鹽酸的質(zhì)量+碳酸鈉溶液的質(zhì)量-放出的二氧化碳的質(zhì)量�。雖然兩個(gè)反應(yīng)中溶液的總質(zhì)量都減少,但原因不同��,一個(gè)是因?yàn)榉磻?yīng)中產(chǎn)生沉淀�,一個(gè)是因?yàn)榉磻?yīng)中放出氣體
文章來源:工業(yè)鹽酸廠家 佛山工業(yè)鹽酸 廣州工業(yè)鹽酸 www.liveharddieyoung.com 提供的信息